A estratégia é promissora para apontar novas terapias para doenças tropicais negligenciadas
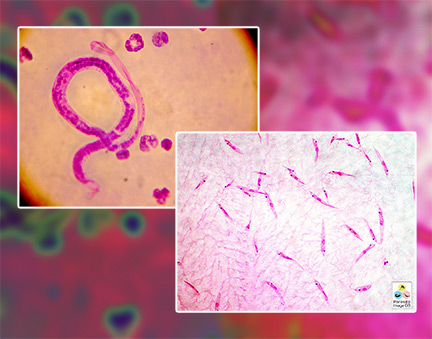
Pesquisadores do INCT do Centro de Química Medicinal de Acesso Aberto sediado no Centro de Química Medicinal (CQMED) da Unicamp avançaram no estudo de uma proteína que ocorre em dois organismos que provocam doenças tropicais negligenciadas. Trata-se da Brugia malayi, um dos vermes causadores da elefantíase (filariose linfática), e da Leishmania major, que provoca a leishmaniose cutânea. A proteína-alvo do estudo, a desoxihipusina sintase (DHS), está relacionada com processos básicos de funcionamento da célula e é inédita como alvo para medicamentos. A busca por inibidores destes processos é um dos caminhos mais prósperos para o desenvolvimento de medicamentos eficazes no tratamento destas doenças. O estudo foi publicado no último dia 22 de outubro na revista científica PLOS Neglected Troppical Diaseases.
Uma das estratégias de descoberta de novas drogas é baseada na identificação de alvos moleculares, muitas vezes uma proteína com atividade enzimática, e no desenvolvimento de inibidores para interromper os processos bioquímicos envolvidos na doença. Esta abordagem baseada em inibidores específicos e potentes é o primeiro passo para elaboração de sofisticados fármacos mais eficazes e de menores efeitos colaterais. O tempo entre a descoberta de novas drogas até a chegada nas prateleiras da farmácia é estimado em 12 a 15 anos e o investimento pode chegar a US$2,5 bilhões. Quando se trata das Doenças Tropicais Negligenciadas (DTNs) este quadro se acentua. A carência de medicamentos desenvolvidos especificamente para o tratamento destas doenças é grande e, muitas vezes, os efeitos colaterais não são desprezíveis.
Duas doenças negligenciadas com necessidades urgentes de novos tratamentos são a leishmaniose, causada por parasitas Leishmania, e a elefantíase, causada pelos nematódeos Wuchereria bancrofti, Brugia malayi e Brugia timori. “Os tratamentos atuais para as três principais manifestações clínicas da leishmaniose (cutânea, mucocutânea e visceral) têm efeitos colaterais graves e muitos são atualmente ineficazes devido ao surgimento de resistência. Para a filariose linfática, os esforços de erradicação têm sido dificultados pela incapacidade dos medicamentos atuais de matar os vermes adultos”, explicam os autores no artigo. Atualmente, existem aproximadamente 70 milhões de pessoas infectadas com vermes filarioses e até 1,6 milhões de novos casos de leishmaniose a cada ano.
No estudo publicado pelo grupo de brasileiros, dois avanços importantes são registrados para entender o funcionamento destas doenças e encontrar possíveis medicamentos. O primeiro refere-se à padronização de uma plataforma de estudo da proteína para o protozoário Leishmania major. O sistema foi baseado em células de levedura que foram modificadas geneticamente para produzir a proteína desoxihipusina sintase (DHS) de Leishmania major. Os pesquisadores verificaram que as leveduras modificadas passaram a depender desta enzima para sobreviver, como é o caso do próprio protozoário. O próximo passo é fazer uma busca de moléculas já conhecidos, para testar quais vão impedir a proliferação da levedura com o gene DHS do protozoário. “A padronização da plataforma de estudo da proteína DHS de Leishmania major baseada em leveduras é fundamental, pois até então não havia sucesso por meio das técnicas convencionais com obtenção desta enzima a partir de outras fontes”, explica Suelen Silva doutoranda do Programa de Biotecnologia da Unesp de Araraquara, bolsista CNPq e a primeira autora do artigo.
O outro avanço descrito no artigo é a determinação da estrutura tridimensional da proteína DHS do verme da elefantíase cuja viabilidade celular depende do bom funcionamento desta enzima. “Embora as proteínas DHS sejam semelhantes, cada organismo carrega uma particularidade. São estas particularidades que nos interessam. É ali que vamos inserir um inibidor. Do contrário, nosso inibidor pode atingir, por exemplo, a proteína do hospedeiro simultâneamente e perdemos especificidade pelo parasita”, explica a coautora Angélica Klippel, doutoranda do Programa de Biociências e Biotecnologia Aplicadas à Farmácia da Unesp de Araraquara e bolsista da FAPESP. Desvendar a estrutura tridimensional da molécula possibilita desenhar inibidores específicos para esta proteína. Com esta estrutura, os pesquisadores investigam os melhores sítios na molécula onde um inibidor poderia se ligar.
Entretanto, como ressaltam os autores no artigo, o fato de identificar um gene, ter sucesso nos ensaios celulares, descrever a estrutura tridimensional da proteína e encontrar um inibidor potente sob condições laboratoriais controladas, não significa automaticamente que o inibidor funcionará dentro do hospedeiro humano. “É um longo percurso, mas cada passo bem sucedido é uma vitória”, explica Rafael Couñago, coautor do estudo e pesquisador principal do Centro que Química Medicinal (CQMED) que hospeda o INCT.
“Neste sentido, a utilização de uma plataforma de levedura que seja útil para o rápido rastreamento em larga escala de novos inibidores destas enzimas poderia contribuir de forma fundamental para o desenvolvimento de possíveis novos fármacos”, destaca o professor Cleslei Zanelli, da Faculdade de Ciências Farmacêuticas da Unesp de Araraquara, pesquisador principal do INCT e coautor do estudo.
Além das enzimas DHS de patógenos da filariose e leishmaniose, os pesquisadores do INCT também estão estudando a estrutura da proteína DHS de outras espécies causadoras de doenças negligenciadas. Com este estudo, os autores esperam facilitar a identificação e o desenvolvimento de novos inibidores de DHS que possam ser usados para validar essas enzimas como alvos para intervenções terapêuticas contra infecções por Brugia malayi e Leishmania major.
A pesquisa está inserida no projeto temático INCT de Química Medicinal de Acesso Aberto que fica no Centro de Química Medicinal (CQMED) da Unicamp e é financiado pela Fapesp, CNPq e CAPES. A principal missão do INCT é fomentar parcerias entre pesquisadores de diferentes centros de pesquisa para investigar proteínas pouco estudadas e assim aumentar o impacto das descobertas. “É um modelo ganha-ganha. Os pesquisadores colaboradores se beneficiam da nossa estrutura e know-how da nossa equipe de pesquisadores totalmente dedicada à bioquímica, biologia celular, molecular e estrutural e química medicinal. E nós aprendemos muito com os desafios que estas colaborações nos trazem”, explica Counãgo.
Participaram ainda pesquisadores do Centro de Biologia Molecular e Engenharia Genética (CBMEG) e Instituto de Biologia, ambos da Unicamp.
Artigo: Silva SF, Klippel AH, Ramos PZ, Santiago AdS, Valentini SR, Bengtson MH, et al. (2020) Structural features and development of an assay platform of the parasite target deoxyhypusine synthase of Brugia malayi and Leishmania major. PLoS Negl Trop Dis 14(10): e0008762.